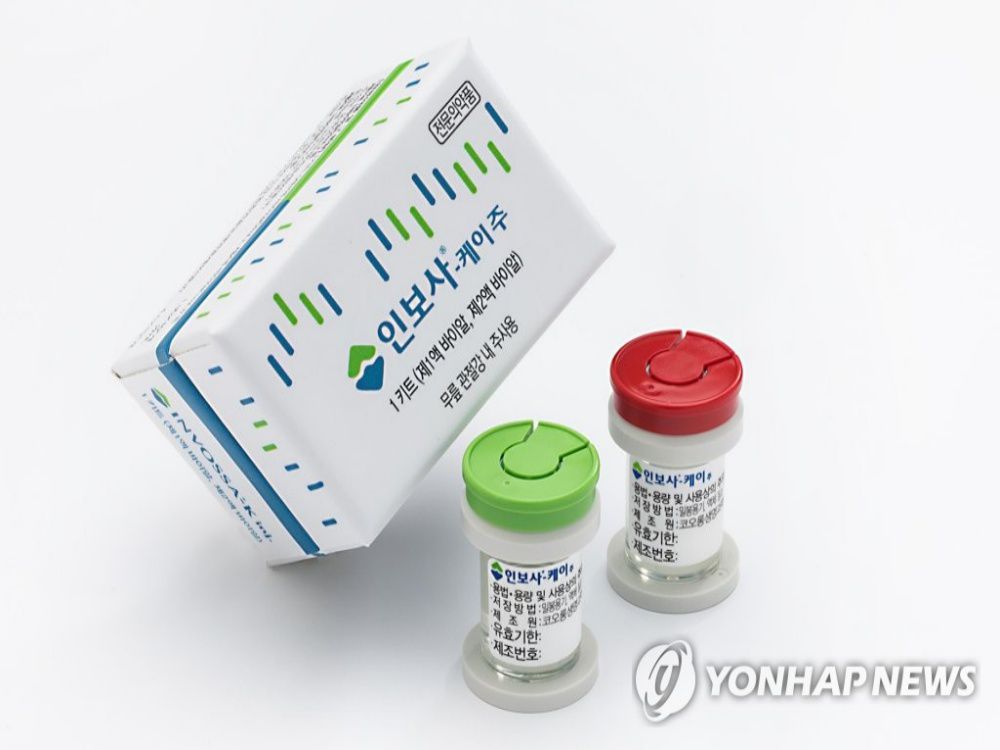
인더뉴스 김진희 기자ㅣ코오롱생명과학이 자사의 골관절염 유전자 치료제 ‘인보사케이주(이하 인보사)’의 품목 허가 취소 처분을 잠정 중단해달라고 법원에 요청했으나 2심 법원에서도 기각됐다.
코오롱생명과학은 24일 공시를 통해 지난 8월 19일 서울행정법원에 제기한 ‘인보사케이주’의 의약품 제조판매 품목허가 취소 효력정지신청 항고가 기각됐다고 밝혔다.
인보사는 코오롱생명과학이 골관절염, 특히 무릎 골관절염 통증 완화를 목적으로 개발한 유전자 세포 치료제(주사제)다. 1액(연골세포)과 2액(연골세포+TGF-β1)으로 이뤄졌다. 세계 첫 유전자 치료제로서 지난 2017년 7월 식약처 허가를 받았다.
그러나 인보사를 구성하는 2액의 연골세포가 종양 유발 가능성이 있는 신장세포인 것으로 확인되면서 지난 5월 식약처는 품목허가를 취소했다.
코오롱생명과학은 식약처 처분에 불복, 지난 7월 행정소송을 제기하며 동시에 처분 효력을 중지해달라는 집행정지를 신청했으나, 8월 이뤄진 판결에서 1심 법원은 취소처분 효력 정지 신청을 기각했다.
회사 측이 주장하는 손해와 식약처의 처분 사이에 명확한 인과관계를 인정하기 어렵고, 현재까지 인보사의 안전성이 의학적으로 검증됐다고 단정할 수 없으며, 집행정지가 인용돼 그에 기초한 다른 조치들이 진행되면 사람의 생명이나 건강에 좋지 않은 영향을 미칠 우려가 있다는 이유에서다. 2심 재판부 역시 1심과 같은 맥락에서 회사 측의 항고를 기각한 것으로 알려졌다.